Il mercato dei pro-ormoni (PH) e dei designer steroids (DS) sta diventando quello fondamentale tra i bodybuilders amatoriali in USA e lo diventerà presto anche per quelli professionistici (lo è già per quelli olimpici, per motivi di aggiramento dell’antidoping). Il motivo di questo sta nell’incrocio tra l’enorme domanda di AAS e la possibilità di aggirare le molto restrittive leggi USA che considerano tutti gli AAS come narcotici. L’inghippo sta nel commercializzare sostanze fuori dall’elenco chiuso del FDA, che poi a sua volta cerca dimostrare che le sostanze in questione sono nocive oppure convertono a testosterone o altre sostanze proibite, oppure di per se costituiscono steroidi anabolizzanti (ma l’onere della prova è carico dell’FDA … e per tutte le cose ci vuole tempo): ne deriva un’ incessante lotta legittima tra commercianti di integratori (così vengono venduti PH e DS) e FDA dove nuovi (di fatto) AAS vengono continuamente inventati, lanciati sul mercato e ritirati (a volte prima che l’FDA intervenga, in modo da poterli ricommercializzare in futuro): in queste condizioni è di fatto impossibile tenere una lista completa dei nuovi prodotti con le loro caratteristiche, anche perché queste caratteristiche rimangono perlomeno quanto mai incerte; a questo contribuisce non solo la velocità del turn over dei prodotti e la mancanza di qualsiasi sperimentazione preventiva, ma anche l’abitudine dei distributori di attribuire alle loro sostanze qualità a volte di fantasia: le verifiche sono quasi impossibili e così spesso ci si imbatte in prodotti semi inerti pubblicitariamente gonfiati, oppure prodotti molto potenti contrabbandati per miti integratori per principianti, questo per ritardare i controlli del FDA o semplicemente perché in un certo momento di questo il mercato fa richiesta.
Dagli USA l’ondata di PH & DS ha già saturato il mercato britannico (dove gli AAS sono legali e questi prodotti sono venduti come integratori senza preoccupazioni di ostracismo da parte delle autorità) … e le prime increspature che annunciano la grande onda sono ormai arrivati anche in Italia.
NEI PROSSIMI ANNI SAPER MANNEGGIARE PH E DS COSTITUIRÀ UN VANTAGGIO TECNICO FONDAMENTALE anche tra i bodybuilders italiani.
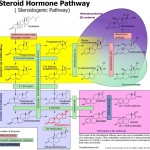
In questa situazione continueremo a pubblicare i profili dei principali PH e/o DS (di fatto sono la stessa cosa), ma prima credo che sia più utile cercare di dare i mezzi tecnici perché ogni utilizzatore possa cercare di capire cosa ha davanti, senza dare troppo peso alle varie informazioni sui forum Usa e UK (spesso pilotate dai distributori). Per fare questo occorre apprendere i rudimenti della chimica androgeno-steroidea e, in particolare, che tipo di modificazioni usano i ricercatori farmacologici per differenziare nuove molecole da quella base di:
TESTOSTERONE (T: definito 100 androgeno/ 100 anabolico e recettorialmente mix).
Le modificazioni più ovvie sono quelle che portano ala formazione di altri ormoni androgeni già presenti nell’organismo umano:
- DEIDROTESTOSTERONE (DHT 100/10, ar). Attraverso l’interazione con l’enzima 5-alfa-reduttasi sul T, questo perde il doppio legame C4-C5 con l’addizione di due atomi di idrogeno alla struttura: questa modificazione crea un aas con un affinità molto più forte del T verso i recettori androgeni, ma che si esplica soprattutto a carico di prostata, clitoride, bulbi piliferi, ghiandole sebacee, mentre a livello muscolare il DHT, prima che possa interagire con i recettori androgeni muscolari, viene degradato dall’enzima 3-alfa-idrodesosi-deidrogenasi (3-alfa-HSD) all’inattivo metabolita androstenediolo. Inoltre il DHT, perdendo, il legame in C4-C5 perde la possibilità di essere aggredito dall’ enzima aromatasi.
- 19-NOR-TESTOSTERONE (NANDROLONE 35/125, ar) differisce dal T soltanto per la mancanza di un carbonio (C) in posizione 19. Il nandrolone deve il suo basso rapporto androgeno/anabolico alla sua potenziale trasformazione, ad opera dell’enzima 5-alfa-reduttasi, nel metabolita deidronandrolone (DHN), scarsamente affine ai recettori androgeni.
Dalla base strutturale di questi 3 AAS naturali, si può passare ad altre tipiche modificazioni per conferire particolari proprietà alla molecola AAS:
1. La più comune è la metilazione, cioè l’aggiunta di un metile ad uno degli atomo di carbonio, allo scopo di aumentarne la biodisponibilità, specialmente orale, permettendo ad una certa quantità di prodotto di superare indenne la barriera epatica. Ci sono vari tipi di metilazione che hanno effetti molto variabili anche su altre caratteristiche della molecola, a prescindere dalla biodisponibilità. comunque le 3 metilazioni più comuni sono le seguenti:
- La più nota è quella della metilazione in C-17. Le sole caratteristiche certe di questa modificazione sono costituite da una forte resistenza alla distruzione a livello epatico e da una diminuzione della velocità interazione con l’enzima aromatasi che però è compensata sovrabbondantemente (dal punto di vista dell’attività estrogenica) dalla metabolizzazione a 17-alfa-metilestradiolo, 5 volte più affine al recettore estrogeno dello stesso estradiolo. Inoltre è consueta una diminuzione variabile dell’affinità verso l’SHBG, cosa che rende la molecola più bioattiva. La resistenza al metabolismo epatico apportata da questo tipo di metilazione è sempre portatrice di notevole stress epatico. La potenza della molecola che ne deriva è molto variabile, in funzione soprattutto della stabilità che apporta al chetogruppo in C-3, vitale per la resistenza al 3-alfa-HSD dei metaboliti 5-alfa-ridotti, e quindi per l’efficacia di questi nei tessuti muscolari. L’incremento di questo aspetto può essere modesto come nel caso del metiltestosterone o assolutamente sconvolgente come nel caso del metiltrenbolone;
- un’altra comune metilazione è quella nella posizione C-1, vantaggiosa perchè apporta una certa resistenza al metabolismo epatico senza stress per quest’organo, ma pressoché incapace nell’incrementare la stabilità del C-3 cheto-gruppo, che rimane piuttosto facilmente aggredibile dall’ 3-alfa-HSD. L’affinità per l’SHBG rimane alta;
- metilazione nella posizione C-2, meno efficace nell’aumentare la resistenza al passaggio epatico rispetto alle C-17 e C-1, ma usualmente efficiente nello stabilizzare il C3-chetogruppo;
- metilazione nella posizione C-7, debole nel difendere la molecola dal passaggio epatico, è più utile nel diminuire l’affinità per l’SHBG ed è in grado di inibire completamente la 5-alfa – riduzione.
2. La 17-alfa-etilazione, che assicura il passaggio epatico al pari della metilazione in C-17, ma con minore stress epatico, ma a costo di uno spiccato incremento per i recettori progestinici.
3. Sostituzione del cheto gruppo in C-3: anziché cercare soluzioni per aumentare la resistenza di questo gruppo all’ 3-alfa-HSD, a volte si provvede a sostituirlo con una configurazione che consenta un legame con il recettore androgenico non aggredibile dall’3-alfa-HSD.
Queste sono le modificazioni più comuni degli AAS, ce ne sono però alcune specifiche o più rare che si sono dimostrate particolarmente efficaci e che si potranno ritrovare tra i PH/DS:
- Sostituzione in C-2 di una molecola di ossigeno, con notevole resistenza all’ossidazione del C-3 cheto-gruppo: tra gli AAS tradizionali è la modificazione unica dell’oxandrolone.
- L’utilizzo in C-2 di un gruppo idrossimetilico con forte stabilizzazione del chetone in C-3: modificazione tipica dell’ossimetolone
- L’introduzione di un doppio legame in C9-C10 inibisce l’aromatizzazione dei composti non 5-alfa-ridotti (es. trenbolone)
- L’insaturazione in C11-C12 aumenta l’affinità per i recettori androgeni dei derivati del nandrolone (es. trenbolone)
Mi scuso per la pesantezza dell’esposizione, ma non ho trovato altro modo per iniziare ad affrontare il tema in modo sistematico. Di fronte a PH e DS non possiamo fare come molti di noi hanno fatto ad inizio di carriera, cioè imparando a memori la tavola degli AAS: la tavola di PH & DS non è un tavola, bensì un ameba in continua espansione e mutazione.
Pietro Sassi
________________

Quest’opera è distribuita con Licenza Creative Commons Attribuzione – Non commerciale – Non opere derivate 3.0 Italia.